Разрушение двойного электрического слоя частиц азопигмента
Аннотация
Приведены результаты исследования природы и энергии связи между ионами водорастворимых примесей, и твердыми частицами органического вещества – азопигментов. Установлено что ионы водорастворимых примесей сорбированны на поверхности частиц твердой фазы. Предложена модель образования двойного электрического слоя, из ионов водорастворимых примесей, вокруг частицы органического вещества. С помощью программного обеспечения «Firetly» рассчитаны энергии связи ионов водорастворимых примесей и частиц азопигментов оранжевого Ж и красного FGR. Предложен механизм разрушения двойного электрического слоя методом введения в систему наночастиц металлов формирующих вокруг себя конкурирующий сорбционный слой ионов водорастворимых солей и способ разрушения этого слоя методом многократной репульпацией-декантацией артезианской водой содержащей металлы никеля, алюминия, железа и платины в наноструктурированной форме. Заключающийся в переходе ионов водорастворимых примесей с поверхности частиц органического вещества на поверхностьметаллов в наноструктурированной форме.
Ключевые слова: частица органического вещества, азопигменты, наночастица, металлы в наноструктурированной форме, многократная репульпация-декантация, двойной электрический слой, ионы, водоасвтроримые примеси
05.17.03 - Технология электрохимических процессов и защита от коррозии
В производстве азопигментов процессы диазотирования и азосочетания параллельно с целевым веществом образуют соли натрия, калия и кальция. Для обеспечения требуемой кислотности среды в реакционную массу вводят кислоты или щелочи [1]. Кислоты с образовавшимися солями в жидкой фазе реакционной массы диссоциируют на ионы [2], наиболее распространенными среди них являются положительно заряженные ионы: водород, натрий, калий, кальций, отрицательно заряженные ионы - хлор, сульфатная группа. При образовании твердых частиц целевого вещества ионы формируют вокруг них координационный слой, состоящий из отрицательно заряженный ионов сорбированных на поверхности частиц органического вещества (потенциалообразующий слой) и расположенных на незначительном расстоянии положительно заряженных ионов (слой противоионов), ионы несорбированные на поверхности частиц твердой фазы образуют диффузионный слой в объеме жидкой фазы, то есть формируется двойной электрический слой [3,4] рис.1.

Рисунок 1 Модель двойного электрического слоя для частиц органического вещества; 1- частицы органического вещества; 2 – отрицательно заряженные ионы; 3 – положительно заряженные ионы; 4 – потенциалопределяющая область; 5 – область расположения проитивоинонов; 6 – диффузионная область.
При удалении примесей (ионов солей и кислот) отмывкой сформировавшегося осадка на фильтрующей перегородке или многократной декантацией суспензии с последующей репульпацией, выводятся ионы из диффузионного слоя и часть ионов из потенциалообразующего слоя величина энергии связи которых с твердыми частицами органического вещества незначительна. То есть, достичь полного удаления водорастворимых примесей (ионов солей и кислот) из суспензий азопигментов используя традиционные методы очистки невозможно.
Для полного удаления водорастворимых примесей из суспензий азопигментов, необходимо в жидкой среде суспензии сформировать условие обеспечивающее разрушение связи ионов находящихся в потенциалообразующем слое частиц органического вещества. Для разрушения связи ион- частица органического вещества, было предложено по окончании процесса удаления ионов из диффузионного слоя в жидкую фазу вводить нанометаллы формирующие активные центры координирующие вокруг себя ионы содержащиеся в двойном электическом слое, при чем энергия связи наночастица металла – ион выше чем энергия связи частицы органического вещества с ионами. В качестве металлов в наноструктурированной форме использовали алюминий, никель платина с размером частиц 15-50 нм.
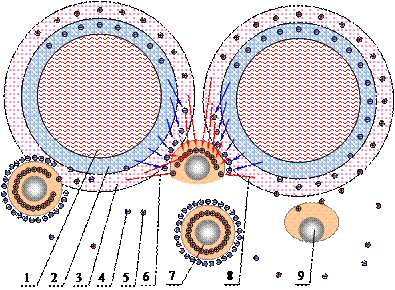
Рисунок 2 Модель разрушения двойного электрического слоя частиц органического вещества за счет перехода ДЭС ионов водорастворимых примесей на поверхность наночастиц; 1 – частицы органического вещества; 2 – потенциалопределяющая область; 3 – область расположения противоионов; 4 – отрицательно заряженные ионы; 5 – положительно заряженные ионы 6 – направление миграции положительно заряженных ионов; 7 – наночастица с ДЭС; 8 – направление миграции отрицательно заряженных ионов; 9 – наночастица.
Предлагаемый способ отмывки тонкодисперсных частиц органических веществ заключается в многократной декантации-репульпации суспензии азопигмента. Первую и вторую репульпации проводили с использованием в качестве промывной жидкости – воды артезианской объемом равным объему жидкой фазы содержащейся в сгущенной суспензии полученной при отстаивании суспензии азопигмента. Температура промывной жидкости 30 ºС так как более высокая температура ведет к повышению растворимости и смачиваемости азопигмента, и как следствие к увеличению потери целевого вещества.
Третью репульпацию осуществляли следующим образом: в сгущенную суспензию вводили промывную жидкость – артезианская вода содержащая наноматериалы – сорбенты ионов водорастворимых примесей в таком же объеме как и при первых двух репульпациях при температуре 30 ºС. Металлы в наноструктурированной форме на своей поверхности из ионов водорастворимых примесей, формируют двойной электрический (рисунок 2). Перераспределение ионов осуществляется при перемешивании суспензии в течении 5-30 мин.
Для удаления мицелл, представляющих собой частицы наноматериалов с сорбированными на их поверхности ионами водорастворимых примесей, при формировании органического слоя над водным слоем, в суспензию вводят коагулянты, обеспечивающие осаждение мицелл в процессе декантации. В случае осаждения органического слоя, удаление частиц наноматериалов возможно фильтрованием суспензии с последующей промывкой на фильтровальной перегородке или проведение четвертого цикла декантации-репульпации.В качестве нанометаллов, использовались, порошки наночастиц алюминия с размером частиц 15-50 нм, платины с размером частиц 15-50 нм, железа с размером частиц 15-50 нм, никеля с размером частиц 15-50 нм. В качестве коагулянта может быть применен полиоксихлорид алюминия PAC (PAX-PS), титановый коагулянт (ТУ 262212-001-45527070-2001), гидроксохлорид алюминия (ТУ 6-00-05795731-250-96), сульфат алюминия (ГОСТ 12966-85).
Способ удаления водорастворимых примесей многократной декантацией-репульпацией был реализован при очитки суспензий Пигментов оранжевого Ж и красного FGR (рисунок 3)
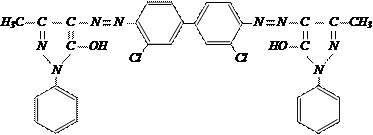 ,
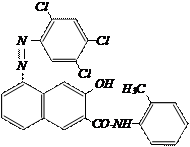
, 
а б
Рисунок 3 Структура азопигмента: а - оранжевого Ж; б - красного FGR,
В качестве водорастворимых примесей при синтезе пигмента оранжевого Ж образуются соли NaCl, Na2SO4, а так же в суспензии азопигмента присутствует HCl, H2SO4, получение пигмента красного FGR сопровождается образованием солей NaCl, Na2SO4, в качестве кислоты суспензия содержит HCl. Состав ионов содержащихся в жидкой фазе этих азопигментов одинаков и состоит из Н+, Na+, Cl-, SO42-. Согласно теории формирования ДЭС вокруг частицы органических веществ [5] формируется потенциалоопледеляющий слой за счет отрицательно заряженных ионов, а слой противоионов соответственно из положительно заряженных. На основании анализа величин энергии связи ионов хлора и сульфатной группы с частицами Пигмента оранжевого Ж и красного FGR рассчитанных при помощи пакета программ Firetly, наиболее вероятным будет формирование потенциалоопледеляющего слоя ионами хлора, а слоя противоионов ионами натрия. Иноны сульфагруппы и водорода будут в основном размещены в диффузионном слое.
При максимальном удалении ионов водорастворимых примесей из диффузионного слоя в суспензию вводятся наночастицы никеля и алюминия размером 15-50 нм., согласно выполненному расчету энергия связи ион – наночастица металла на 18-47% выше чем энергия связи ион – частица азопигмента (таблица 1).
Таблица 1. Значения энергии связи рассчитанные с помощью программы Firetly
|
№ |
Наименование связи |
Ед. изм. |
Значение |
|
1 |
Пигмент оранжевый Ж-ион хлора |
кДж/моль |
156 |
|
2 |
Пигмент оранжевый Ж- сульфат ион |
кДж/моль |
47 |
|
3 |
Пигмент красный FGR- ион хлора |
кДж/моль |
118 |
|
4 |
Пигмент красный FGR- сульфат ион |
кДж/моль |
34 |
|
5 |
Наночастица никеля - ион натрия |
кДж/моль |
196 |
|
6 |
Наночастица никеля- ион водорода |
кДж/моль |
98 |
|
7 |
Наночастица алюминия - ион натрия |
кДж/моль |
171 |
|
8 |
Наночастица алюминия - ион водорода |
кДж/моль |
71 |
|
9 |
Наночастица железа - ион натрия |
кДж/моль |
192 |
|
10 |
Наночастица железа - ион водорода |
кДж/моль |
91 |
|
11 |
Наночастица платины - ион натрия |
кДж/моль |
224 |
|
12 |
Наночастица платины - ион водорода |
кДж/моль |
124 |
Реализация вышеизложенного способа удаления водорастворимых примесей из суспензий азопгименов оранжевого Ж и красного FGR с использованием в качестве промывной жидкости на третьем цикле репульрации-декантации артезианской воды содержащей наночастицы железа, никеля или платины с концентрацией 5×10-3 кг/м3 позволила получить следующие результаты эффективности удаления примесей с поверхности частиц органического вещества (таблица 2).
Таблица 2. Эффективность удаления водорастворимых примесей
|
Наночастицы используемые при репульпации |
Общее количество промывных вод, м3 |
Характеристики отмытой сгущенной суспензии |
|
|
Концентрация водорастворимых примесей в жидкой фазе, кг/м3 |
Концентрация водорастворимых примесей сорбированных на твердой фазе, кг/м3 |
||
|
Пигмент оранжевый Ж |
|||
|
Без наноматериала* |
66 |
0,35 |
0,18 |
|
Железо |
44 |
0,21 |
0,10 |
|
Никель |
44 |
0,22 |
0,10 |
|
Платина |
44 |
0,21 |
0,09 |
|
Пигмент оранжевый FGR |
|||
|
Без наноматериала* |
70 |
0,30 |
0,17 |
|
Железо |
40 |
0,28 |
0,09 |
|
Никель |
40 |
0,29 |
0,10 |
|
Платина |
40 |
0,27 |
0,07 |
*- процесс многократной репульпации–декантации осуществлялся до достижения требуемой концентрации водорастворимых примесей в пасте азопигментов с использованием на каждом цикле объема воды равного объему сгущенной суспензии, (количество циклов для Пигмента оранжевого Ж - 6, для Пигмента красного FGR – 7).
На основании полученных данных (таблица 2), можно сделать следующие выводы:
1.Использование при отмывке тонкодисперсных органических продуктов многократной репульпации-декантации водами содержащими наночастицы металлов позволяет снизить количество промывных вод на 40-43%, при одновременном повышении характеристик качества (колористическая концентрация) на 20-40%.
2.Максимальная эффективность процесса разрушения ДЭС у частиц азопигмента обеспечивается наночастицами платины, а так же наночастицами железа или никеля.
Список литературы
1.Степанов, Б. И. Введение в химию и технологию органических красителей / Б. И. Степанов. - М.: Химия, 1984. - 592 с.
2.Захарченко В.Н. Коллоидная химия. – 2-е изд., перераб. - М.: Высшая школа. 1989г. – 237с.
3.Салем Р.Р. Теория двойного электрического слоя. - М.: Физматлит, 2003. – 104с.
4.Статья Маши
5.Мягченков В.А. Поверхностные явления и дисперсные системы. М.: КолосС. 2007. - 187 с.