Синтез и электрохимические характеристики нового композитного катодного материала LiMn2O4/LiCoO2 для литий-ионных аккумуляторов
Аннотация
Дата поступления статьи: 15.06.2014Композитный катодный материал типа ядро/оболочка с формулой LiMn2O4/LiCoO2 успешно синтезирован с помощью метода твердофазных реакций в несколько этапов. Структура его исследована с помощью рентгеновской дифракции, растровой и просвечивающей электронной микроскопии, а также колебательной инфракрасной спектроскопии. Электрохимическое исследование в двухэлектродной ячейке показало улучшение характеристик синтезированного катодного материала по сравнению с составляющими компонентами. Удельная мощность LiMn2O4@LiCoO2 составляет 650 мВтч/г, против 450 и 500 мВтч/г у LiMn2O4 и LiCoO2 соответственно.
Ключевые слова: литий-ионные аккумуляторы, композитные катодные материалы, рентгеностуктурный анализ, электронная микроскопия, электрохимические свойства
Введение
В последние несколько лет активно развивается технология новых композитных катодных материалов для литий-ионных аккумуляторов, обеспечивающих большую, по сравнению с компонентами удельную емкость, лучшую стабильность при многократном циклировании [1 − 7]. Для достижения указанных целей существует ряд путей, таких как переход к наноматериалам, легирование и синтез твёрдых растворов, и создание гетероструктурных систем типа ядро/оболочка [6, 7]. Отметим также незатухающий научный интерес к гетероструктурам [8].
Целью нашей работы является получение и электрохимическое исследование композита на основе известных катодных материалов LiMn2O4 и LiCoO2 [1] в структурированной форме ядро/оболочка, где ядром служит кристаллит LiMn2O4, окружённый оболочкой, состоящей из LiCoO2.
Методика эксперимента
Рентгеноструктурный и рентгенофазовый анализ полученных образцов проведен с помощью дифрактометра ARL-X’TRA методом Брегга-Брентано (θ − 2θ). Съёмку вели в пошаговом режиме, при комнатной температуре в интервале углов 2θ = 10°–70° с шагом сканирования 0,02°. Время экспозиции на каждом шаге 1 с. Использовано излучение CuKα1 − анода с длиной волны 1,5406 Å.
Спектры инфракрасного отражения от порошкообразных образцов, приготовленных в виде прессованных таблеток с бромидом калия KBr, получены с использованием инфракрасного Фурье-спектрометра ФСМ-1202 в диапазоне частот 400 − 1000 см−1 со спектральным разрешением 0,5 см−1.
Для определения морфологии и размеров частиц получены изображения исследуемых объектов на растровом электронном микроскопе Zeiss Supra 25 в режиме отраженных электронов.
Для проведения просвечивающей электронной микроскопии (ПЭМ) препарат в количестве 0,5 г насыпали в емкость с двумя миллилитрами 50% этилового спирта, затем емкость помещали в ультразвуковую ванну и обрабатывали ультразвуком мощностью 1 Вт в течение 15 мин. Полученную взвесь в виде капли помещали на подложку из тонкой формварной плёнки (~ 100 нм). Плёнка, в свою очередь уже была смонтирована на медную сетку-подложку для ПЭМ. Препарат оставляли при комнатной температуре до полного высыхания. Далее сеточки помещались в трансмиссионный электронный микроскоп марки Tecnai G2 Spirit BioTWIN и изучались в проходящем пучке электронов с ускоряющим напряжением 100 кВ в светлопольном режиме. Такое ускоряющее напряжение для металлофизических исследований позволяет просвечивать электронным лучом объекты, толщиной до 2 мкм. Для того чтобы исследуемый образец не нагревался от электронного луча, его охлаждали при помощи жидкого азота.
Приготовление композитного материала LiMn2O4/LiCoO2
Композитный материал LiMn2O4@LiCoO2 был получен методом твердофазных реакций в два этапа. На первом этапе был проведён синтез материала ядра, т.е. LiMn2O4.
Соотношение масс ядро: оболочка выбрано 1:10, т.к. в этом случае имеется наибольшая вероятность того, что кристаллы ядра будут выступать центрами кристаллизации при синтезе материала оболочки, т.е. оболочка будет образовываться на ядре [4 − 7].
Литий марганцевую шпинель LiMn2O4 получали твердофазным взаимодействием карбоната лития Li2CO3 с оксидом марганца (III) Mn2O3. По реакции:
2Li2CO3 + 4Mn2O3 + O2 → 4LiMn2O4 + 2CO2
Смесь исходных компонентов, взятых в стехиометрических количествах, перетирали со спиртом в яшмовой ступке, прессовали в цилиндрические таблетки и обжигали в муфельной печи при 900оС в течение 3 часов на воздухе.
На втором этапе для получения композитного материала LiMn2O4/LiCoO2 однофазный кристаллический LiMn2O4 смешивался в шаровой мельнице планетарного типа Fritch со стехиометрической смесью прекурсоров Li2CO3 и CoO для получения LiCoO2 с соотношением масс LiMn2O4 – LiCoO2 как 1:10. Смешивание проводили в планетарной шаровой мельнице в течение 30 минут при скорости 400 об/мин в этилацетате. Выбор этилацетата обоснован тем, что он не содержит воды, в нём не растворяются компоненты смеси прекурсоров, и он легко удаляется выпариванием. Затем проводился синтез композита в муфельной печи при 900 – 950оС в течение 1 часа.
Также для контроля была приготовлена механическая смесь кристаллических фаз LiMn2O4 и LiCoO2 в весовом соотношении 1:10 соответственно.
Результаты и обсуждение
Рентгенофазовый анализ механической смеси показал наличие компонентов в заданных соотношениях.
На рентгенограммах приготовленного композитного материала LiMn2O4/LiCoO2 выявляются дифракционные отражения лишь кобальтита лития, находящегося в оболочке композита LiMn2O4/LiCoO2. При этом рентгеновское излучение от внутренней фазы, т.е. ядра LiMn2O4 поглощается (рис.1) и не наблюдается на рентгенограммах.
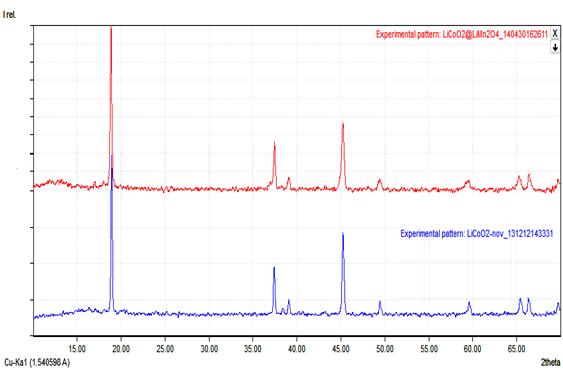
Рис.1. − Рентгенограммы LiMn2O4/LiCoO2(вверху) и LiCoO2 (внизу)
Рентгеноструктурный анализ целевого продукта был проведён с использованием программного пакета FullProf 2014. Для уточнения структуры были использовано 16 параметров и гауссова форма пика, а именно 6 параметров, относящихся к структуре и 10 профильных параметров. Значения параметров после уточнения приведены в таблице №1 в сравнении с кобальтитом лития [9], значения профильного R-фактора составило 8 %.
Таблица №1
Сравнение параметров чистого LiCoO2 и в LiMn2O4/LiCoO2
|
LiMn2O4/LiCoO2 |
LiCoO2 |
Пр. группа |
R-3m, № 166 |
R-3m, № 166 |
a=b, Å |
2,807 |
2,817 |
c, Å |
14,082 |
14,052 |
V, Å3 |
96,09 |
96,57 |
c/a |
5,017 |
4,988 |
Число формульных единиц |
3 |
3 |
z(O2-) |
0,2609 |
0,2538 |
Отметим некоторое уменьшение объема ячейки LiCoO2 и увеличение полуширин дифракционных отражений в композитном составе, что, вероятно, связано со взаимодействием с внутренним ядром LiMn2O4 и ростом, вследствие этого, степени дефектности оболочки.
ИК-спектры композита LiMn2O4/LiCoO2 в сравнении с керамикой LiCoO2 приведены на рис.2. В соответствии с теоретико-групповым анализом число активных колебаний в ИK-спектрах LiCoO2 равно 4 [10, 11]. В спектре LiCoO2 полосы колебаний октаэдров LiO6 и CoO6 в соответствующих слоях проявляются раздельно: полосы колебаний CoO6 лежат в области 400−700 см−1, а LiO6 − в области 200−400 см−1 [11, 12].
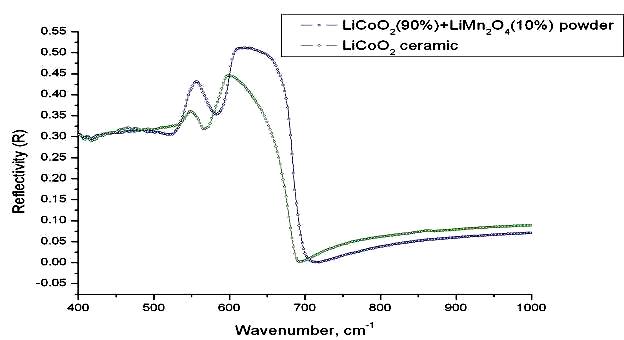
Рис.2. − ИК-спектр LiMn2O4/LiCoO2 и LiCoO2.
В спектре керамики из однофазного LiCoO2 наблюдаются две интенсивные полосы при частотах приблизительно 600 и 520 см−1 (СоО6).
В спектрах структурированного композита LiMn2O4/LiCoO2 присутствуют все те же полосы, что и в керамике LiCoO2, однако интенсивность их существенно выше. Также появляется дополнительная полоса при частоте приблизительно 650 см−1, которую трудно выделить в керамике LiCoO2.
На ИК-спектреLiMn2O4/LiCoO2 наблюдается увеличение интенсивности полос, соответствующих колебаниям СоО6 (рис.2). Увеличение интенсивности полос можно интерпретировать как уменьшение искажения октаэдров [10 − 12]. Следует также отметить наличие слабой полосы колебаний групп CO32- (865 см-1), что вызвано, вероятно, поглощением СО2 из воздуха свежей поверхностью LiCoO2, появившейся в результате его длительного хранения, с образованием карбонатов.
Растровая электронная микроскопия образца композита LiMn2O4/LiCoO2 (рис.3), приготовленного в виде керамики показывает слоистую структуру кристаллитов, наблюдаемую на поверхности керамики LiMn2O4/LiCoO2, которая характерна для кобальтита лития.

Рис.3. − Морфология поверхности композита LiMn2O4/LiCoO2.
Темные границы раздела, наблюдаемые между кристаллитами, указывают на возможную хорошую электронную проводимость таких межзёренных границ. Средний размер кристаллитов композита составляет 1 – 1,5 мкм.
На снимках просвечивающей электронной микроскопии LiMn2O4/LiCoO2 (рис.4 а, б) видны области различной электронной плотности в самих кристаллитах, что показывает сильно неоднородное распределение двух оксидных компонентов LiMn2O4 и LiCoO2.

а
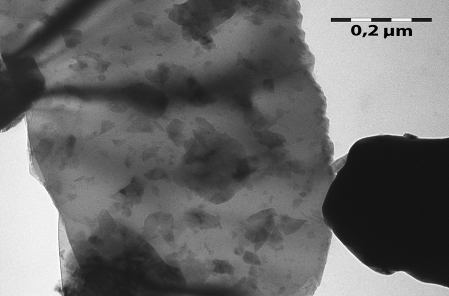
б
Рис.4 а, б. − Микрофотографии просвечивающей микроскопии порошкового образца LiMn2O4/LiCoO2.
Данный факт может указывать на образование структурированного композита типа ядро/кора по типу ядро-оболочка. Следовательно, соотношение 1:10 по массе позволяет, таким образом, достичь окутывания внутренней фазы внешней.
Электрохимические исследования композитного катодного материала LiMn2O4/LiCoO2 (рис.5) показывают его возможность к многократному циклированию в диапазоне напряжений 2,8−4,5 В в гальваностатическом режиме при токах С/10 – 1С (где С – ёмкость аккумулятора в мАч) до разрядно-зарядной ёмкости 180 мА/г ±5%, что составляет 65−70 % от теоретической ёмкости LiCoO2 (270 мАч/г). При этом среднее напряжение разряда составляет 3,95 В.
В тоже время чистый кобальтит лития способен обратимо циклироваться в диапазоне напряжений 2,8−4,2 В при среднем разрядном напряжении 3,7 В и удельной ёмкости 130−140 мАч/г (рис. 6), (что составляет 50% от теоретической ёмкости LiCoO2) при токах С/10 – С/2.
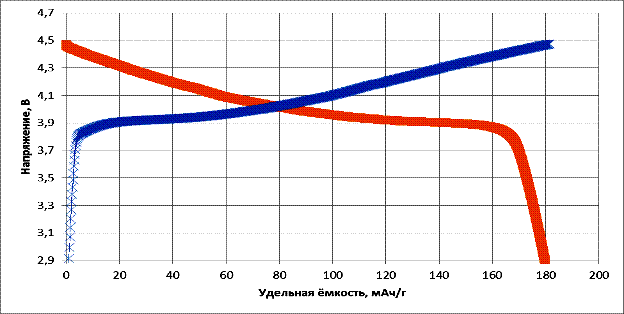
Рис.5. − Зарядно-разрядные кривые композита LiMn2O4/LiCoO2. Заряд – синяя кривая, разряд – оранжевая кривая
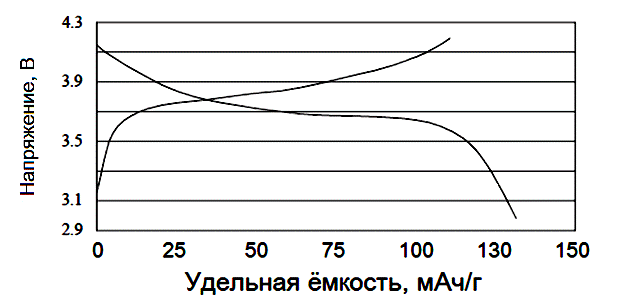
Рис. 6. − Зарядно-разрядная характеристика чистого кобальтита лития
Сравнение разрядной ёмкости при многократном циклировании LiMn2O4/LiCoO2 и LiCoO2 показывает практически небольшое снижение ёмкости в обоих случаях при более высоком значении емкости исследуемого композита (рис.7). Однако для композита наблюдается некоторое падение ёмкости на первом цикле. Этот факт можно объяснить возможными побочными реакциями на поверхности композита с электролитом, в результате увеличения поверхности активного материала [5 − 7].
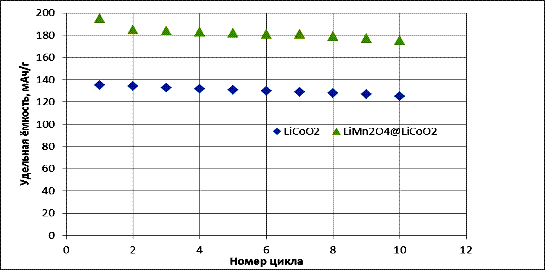
Рис. 7.− Сравнение зависимость удельной ёмкости LiMn2O4/LiCoO2 и LiCoO2
Таблица №2
Сравнение электрохимических свойств LiMn2O4/LiCoO2 с некоторыми катодными материалами
Формула |
Удельная ёмкость, мАч/г |
Среднее напряжение разряда, |
Удельная мощность, Вт/г |
Ток заряда-разряда при КПД не менее 70%, |
LiMn2O4/LiCoO2 |
170 |
3,95 |
670 |
до 1С |
LiMn2O4 |
110 |
4,10 |
450 |
до 5С |
LiCoO2 |
135 |
3,70 |
500 |
до 0,5С |
LiMn1/3Ni1/3Co1/3O2 |
185 |
3,84 |
710 |
до 0,5С |
Как видно из сравнения (таблица №2; рис.5,6,7), описанный нами катодный материал LiMn2O4/LiCoO2 превосходит по электрохимическим параметрам большинство современных катодных материалов, за исключением высокоэффективного LiMn1/3Ni1/3Co1/3O2 . Однако LiMn2O4/LiCoO2 в тоже время обладает улучшенными характеристиками по сравнению с исходными компонентами, а именно LiMn2O4 и LiCoO2.
Выводы
Синтезирован и исследован новый композитный катодный материал типа ядро/оболочка LiMn2O4/LiCoO2. Методами просвечивающей микроскопии установлена его преимущественная связность 0−3, по типу ядро/кора. Показана перспективность его использования в качестве катодного материала для литий-ионных аккумуляторов. Получена удельная разрядная ёмкость до 180 мАч/г в диапазоне напряжений 2,8 – 4,5 В, при токах заряда-разряда до 1С.
Отметим, что создание композитных материалов типа ядро/кора показывает в нашем случае следующие преимущества по сравнению с исходными однофазными катодными материалами: увеличивается среднее разрядное напряжение, т.е. номинальное напряжение источника тока; наблюдается рост величины конечного напряжения заряда, а, следовательно, и мощности; увеличиваются значения допустимого зарядного и разрядного токов.
Литература:
1. Whittingham M.S. Lithium Batteries and Cathode Materials // Chem. Rev., 2004. − V. 104. − № 10. − Р. 4271 − 4301.
2. Фиговский, О. Новейшие нанотехнологии [Электронный ресурс] // «Инженерный вестник Дона», 2012, № 1. – Режим доступа: http://ivdon.ru/magazine/archive/n1y2012/725 (доступ свободный) – Загл. с экрана. – Яз. рус.
3. Клёнушкин, А.А., Медведев, Б.С., Кабиров, Ю.В., Чебанова, Е.В. Синтез и электрохимические свойства твёрдого раствора LiMn1/3Cr1/3Fe1/3O2 со структурой α-NaFeO2 [Электронный ресурс] // «Инженерный вестник Дона»,
2014, № 1. – Режим доступа: http://www.ivdon.ru/magazine/archive/n1y2014/2267 (доступ свободный) – Загл. С экрана. – Яз. рус.
4. Park K.-S., Benayad D. Im. A., Dylla A., Stevenson K., Goodenough J. LiFeO2-Incorporated Li2MoO3 as a Cathode Additive for Lithium-Ion Battery Safety // J. Chem. Mater., 2012. − V. 24. − Р. 2673.
5. Noh J.-K., Kim S, Kim H., Choi W., Chang W., Byun D., Cho B.-W. and Chung K. Y. Mechanochemical Synthesis of Li2MnO3 Shell/LiMO2 (M = Ni, Co, Mn) Core-Structured Nanocomposites for Lithium-Ion Batteries // Scientific Reports, 2014. − V. 4. − Р. 1.
6. Wu F., Li N., Su Y., Shou H., Bao L., Yang W., Zhang L., An R., and Chen S. Spinel/Layered Heterostructured Cathode Material for High-Capacity and High-Rate Li-Ion Batteries // Adv. Mater. 2013, − Р. 1.
7. Su L., Jing Y. and Zhou Z. Li-ion battery materials with core-shell nanostructure // Nanoscale, 2011. − V. 3. − Р. 3967.
8. Алфёров Ж.И. История и будущее полупроводниковых гетероструктур [Текст] // Физика и техника полупроводников, 1998. − Т. 32. − № 1. − C. 1.
9. Безносиков, Б.В., Александров, К.С. Кристаллы семейства делафоссита. [Текст]: Препринт № 843 Ф / Б.В. Безносиков. – Красноярск: институт физики им. Л.В. Киренского СО РАН, 2007. − 32 с.
10. Moore R. K. and White W. B. Study of Order-Disorder in Rock-Salt-Related Structures by Infrared Spectroscopy // J. of American Ceramic Society, 1970. − V. 53. − № 12. − Р. 679.
11. Косова Н. В., Ануфриенко В. Ф., Ларина Т. В., Девяткина Е. Т. Синтез LiCoO2 катодного материала для литий-ионных аккумуляторов с использованием механической активации. [Текст] // Химия в интересах устойчивого развития, 2001. –Т. 9 – № 2. − С. 235.
12. Julien C. Local Environment in 4-Volt Cathode Materials for Li-Ion Batteries // Materials for Lithium-Ion Batteries. – Springer Netherlands, 2000. – V. 85. – С. 309.